人工智能賦能納米分辨CT表征技術,驅動新型納米藥物與細胞技術研發新紀元
在生物醫學研發的前沿領域,新型納米藥物與先進細胞技術的開發正以前所未有的速度推進。其核心挑戰之一在于對納米尺度藥物載體及細胞內部結構的精準、非侵入性表征與定量分析。傳統成像技術往往在分辨率、穿透深度或動態監測能力上存在局限。如今,人工智能與納米分辨計算機斷層掃描(CT)表征技術的深度融合,正為這一瓶頸帶來革命性突破,開啟研發新范式。
一、 納米分辨CT:透視納米世界的“慧眼”
納米分辨CT技術,特別是基于同步輻射或先進實驗室光源的X射線納米CT,能夠以數十納米甚至更高的空間分辨率,對樣本進行三維無損成像。它不僅能清晰呈現納米藥物顆粒的形貌、尺寸分布、孔隙結構及其在載體中的裝載情況,還能在接近生理狀態下,可視化細胞內部的三維超微結構、細胞器分布以及納米藥物與細胞的相互作用過程。這為理解藥物的遞送機制、胞內釋放動力學及生物效應提供了至關重要的直觀證據。
二、 AI賦能:從海量數據中挖掘深層知識
納米CT掃描產生的是包含巨量體素的復雜三維數據集,其處理、分析與解讀極具挑戰性。人工智能,尤其是深度學習技術,在此扮演了“超級大腦”的角色:
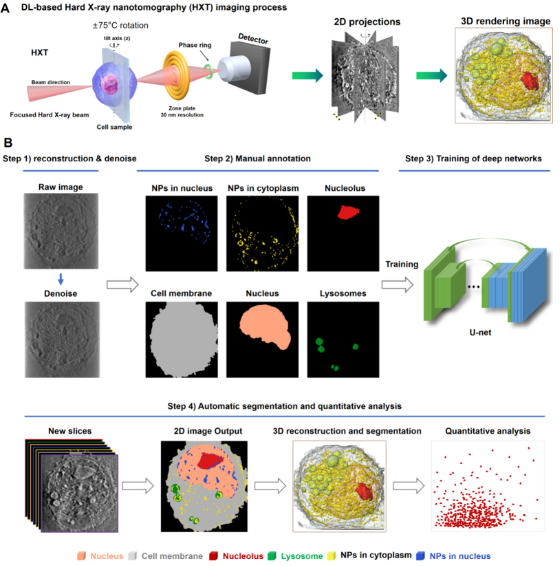
- 圖像增強與重建:AI算法能夠有效降低噪聲、補償缺失數據,從低劑量或欠采樣掃描中重建出高質量圖像,縮短掃描時間并減少輻射損傷,這對于活細胞動態監測尤為重要。
- 自動分割與識別:利用卷積神經網絡(CNN)等模型,AI可以自動、準確地從三維圖像中分割出單個納米顆粒、細胞膜、細胞核、線粒體等特定目標,實現高通量、客觀的形態學與統計學分析。
- 特征提取與關聯分析:AI能超越人眼局限,挖掘圖像中細微的紋理、模式與關聯特征。例如,將納米藥物在腫瘤組織中的空間分布特征與療效數據進行關聯分析,預測其靶向效率;或分析細胞器在藥物刺激下的結構變化模式,揭示其作用機制。
- 預測建模與虛擬篩選:基于大量CT表征數據訓練的AI模型,可以建立納米顆粒結構(如尺寸、形狀、孔隙率)與其生物學性能(如載藥量、釋放曲線、細胞攝取率)之間的預測關系,加速最優納米藥物配方的虛擬設計與篩選。
三、 應用賦能:加速納米藥物與細胞技術研發閉環
1. 在新型納米藥物研發中:
- 理性設計與優化:AI驅動的納米CT分析可精準反饋藥物載體的結構信息,指導合成工藝的調整,實現“結構-性能”的理性設計閉環。
- 體內外行為追蹤:在動物模型或類器官中,動態CT成像結合AI分析,可定量追蹤納米藥物在體內的分布、代謝、靶向聚集及清除全過程,極大提升臨床前研究的效率和預測能力。
- 生物安全性評估:高分辨率地評估納米材料在細胞和器官水平的潛在蓄積與結構影響,為安全性評價提供更精細的依據。
2. 在細胞技術研發與應用中:
- 細胞治療質控:對用于細胞治療的干細胞或免疫細胞(如CAR-T細胞)進行無損三維成像,AI可自動評估其狀態(如活力、分化程度、內部結構健康度),實現生產過程中的在線質控。
- 細胞-材料相互作用研究:在組織工程與再生醫學中,精確分析支架材料的納米結構如何影響細胞粘附、鋪展、遷移及分化,為智能生物材料設計提供指導。
- 疾病模型構建與機制解析:在患者來源的類器官或三維細胞球模型中,利用該技術研究疾病引起的超微結構改變,以及候選藥物如何修復這些異常。
四、 未來展望與挑戰
盡管前景廣闊,AI賦能納米分辨CT技術仍面臨挑戰:需要更多高質量、標注完備的多模態數據來訓練更魯棒、可解釋的AI模型;需要開發更高效的算法以處理實時或近實時數據流;需要跨學科團隊(物理、生物、計算科學、臨床醫學)的緊密協作。
隨著硬件技術的進步(如更亮的源、更快的探測器)與AI算法的持續創新,這一融合技術將變得更加高效、智能和普及。它將不僅僅是一個觀察工具,更將成為驅動納米藥物與細胞技術從基礎發現到臨床轉化全鏈條的智能決策核心,最終為精準醫療帶來突破性療法。
如若轉載,請注明出處:http://m.yijianjiaoyu.cn/product/33.html
更新時間:2026-02-22 00:49:30









